导言
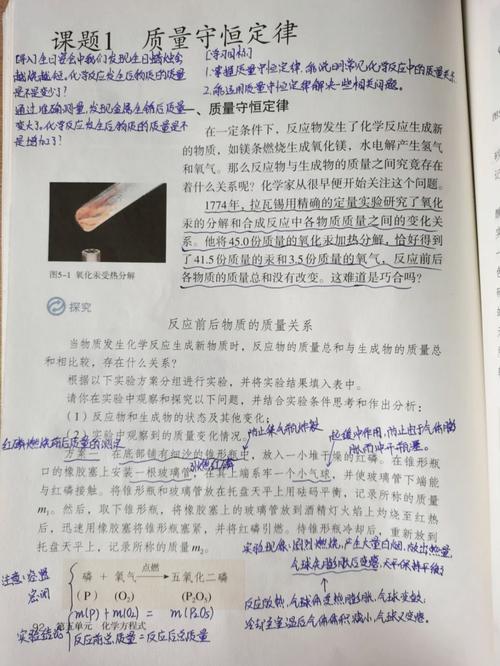
质量守恒定律是自然科学中最基础也是最伟大的定律之一,它揭示了物质在化学变化中不会凭空产生或消失。该定律可以表述为:在一个封闭系统中,系统的总质量保持不变,无论经历多少化学反应或者物理变化,系统总质量不会改变。这一原理不仅对化学领域具有重要意义,而且在物理、环境科学乃至工程学等领域都有着广泛的应用。本文将通过详细的实验视频解析质量守恒定律,帮助读者更直观地理解这一基本化学原理。
实验材料与设备
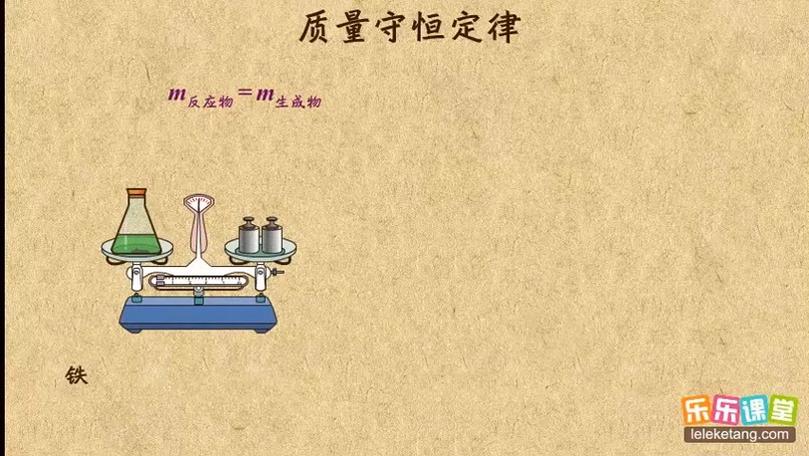
为了体现质量守恒定律的重要性,我们准备了一系列实验设备和材料,包括天平、烧杯、玻璃棒、酒精灯、铁架台、滴管、石棉网、白磷、氧化铜、锌粒及稀硫酸溶液等。这些材料和设备的选择旨在确保实验的准确性和可重复性,同时使实验更加直观。
实验背景
化学反应过程中,反应物通过化学键的断裂和重组转化为产物。尽管反应前后物质的形态可能会发生改变,但这些变化并不会影响系统内总质量的守恒。要验证这一原理,需要选择合适的实验场景。这里选择锌粒与稀硫酸反应作为实验模型。这不仅因为该反应的现象明显,便于观察,而且还能直接测量反应前后的质量变化,从而验证质量守恒定律。此外,该实验还涉及到金属与酸性物质的反应,能够展示不同化学物质间的实际作用,增加实验的实用性。
实验步骤
步骤一
确保烧杯干净且干燥,然后仔细使用电子天平称量烧杯与锌粒的总质量,记录数值。
步骤二
将称量好的锌粒缓缓加入烧杯中,确保锌粒完全浸入稀硫酸溶液中。用玻璃棒轻轻搅拌,促进反应的发生。同时,通过视频记录并观察反应现象,包括气泡产生速率和颜色变化。
步骤三
当反应明显减缓,即大部分锌粒已经反应完毕时,停止搅拌。静置数分钟,让溶液中的任何残留气体完全释放。
步骤四
将烧杯再次置于电子天平上,记录烧杯内所有物质(包括溶液)的总质量。通过前后质量的对比,可以直观地验证质量守恒定律。
数据比较
比较实验前后称量得到的总质量,若无明显误差,则说明实验过程符合质量守恒定律的原理。
结论与讨论
根据实验观察,锌与稀硫酸反应前后,烧杯内总物质质量保持不变。这不仅验证了质量守恒定律的正确性,而且进一步展示了化学反应的本质——质量守恒。实验现象和数据表明,锌粒与稀硫酸反应生成氢气和硫酸锌溶液,整个过程中,化学物质的质量总和保持恒定。从理论上讲,这一实验结果反映了化学反应的本质特征:反应前后的质量守恒。此结论对理解物质转化和化学平衡具有重要意义,为化学教学和科学研究提供了有力支持。
未来展望
质量守恒定律是科学知识体系中的一块基石,其重要性不仅在于验证化学反应的真实性质,更在于它所代表的科学精神——基于观察、实验、推理准确地描述自然现象。未来,实验视频可以通过多元化的技术手段进一步丰富和提升质量守恒定律的教学体验,通过虚拟实验室、增强现实技术等手段,为学生提供更直观、更生动的学习体验,帮助他们更好地理解和应用这一基本化学原理。